ご挨拶
私たちは、2020年6月に東京工業大学生命理工学院の新たな研究室として始動しました。本研究室は、研究領域にとらわれない多角的な解析手法を用いて、がん細胞の悪性形質獲得の分子機序を正確に理解し、基礎研究からトランスレーショナルリサーチに発展させることで、これまでにないがん治療法・診断法の開発を目指しております。
近年、外科手術、放射線療法、薬物療法、免疫療法の進歩により、がん患者の生存率は上昇傾向にあります。しかし、残念ながら、一部の難治がんは早期に転移を起こすため、5年相対生存率は30%に満たないのが実情です。このような難治がんの治療成績を向上させるためには、まず、遠隔転移を制する(理解する)必要があります。
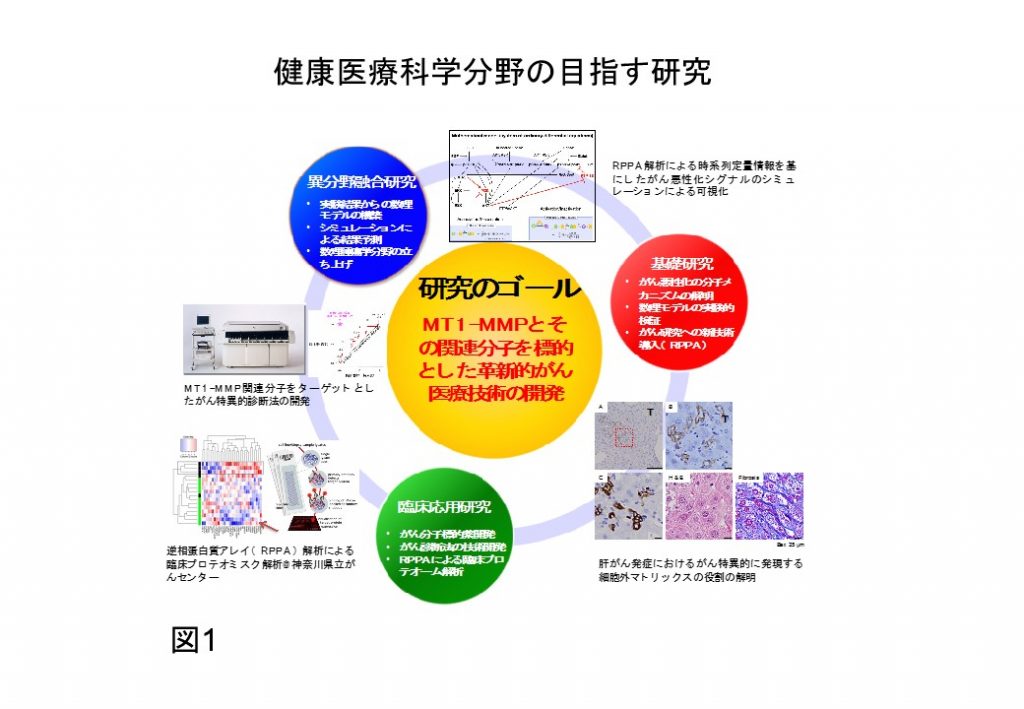
私たちは、先駆的な異分野技術を用いて、これまで一貫して、膜型マトリックス・メタロプロテアーゼ1(MT1-MMP)とその基質に一貫して着目し、MT1-MMP基質蛋白の分解による多様ながんの悪性形質の制御メカニズムを理解することで、MT1-MMPとその関連分子を標的とした革新的がん医療技術の開発を目指しています(図1)。
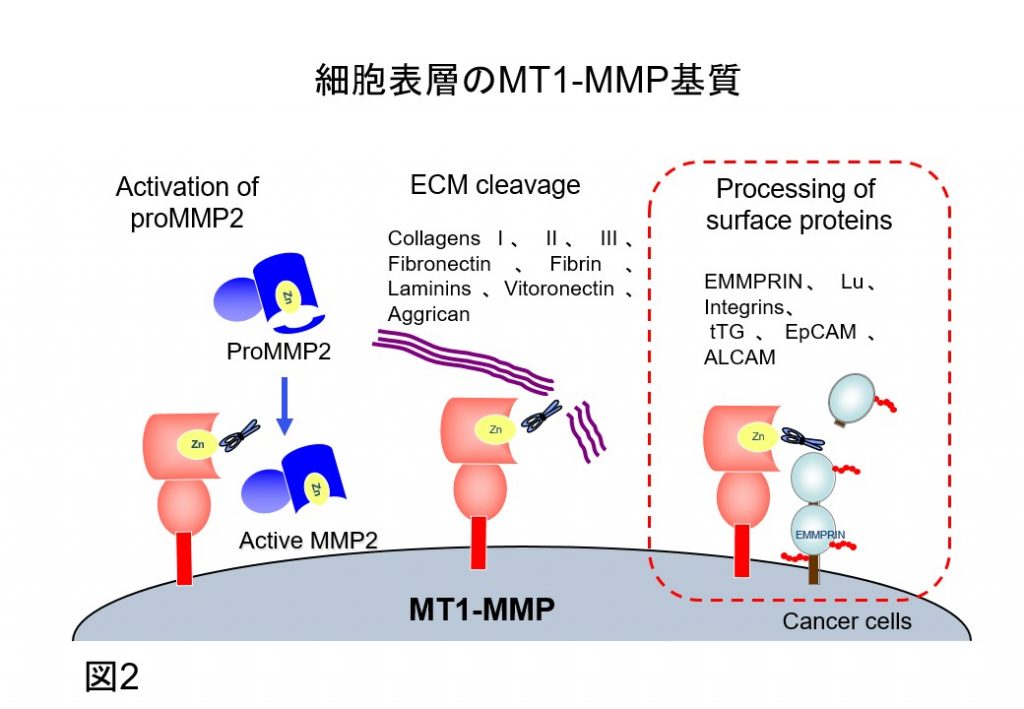
MT1-MMPは1994年に金沢大学の佐藤、清木らによって発見されました。当初、MT1-MMPは浸潤性がんに高頻度に発現し、基底膜破壊に重要なMMP2前駆体の活性化やがん細胞周辺のコラーゲンをはじめとする間質組織構造を破壊することで、MT1-MMPはがん転移・浸潤の動力源として重要とされてきました(図2左、中央)。
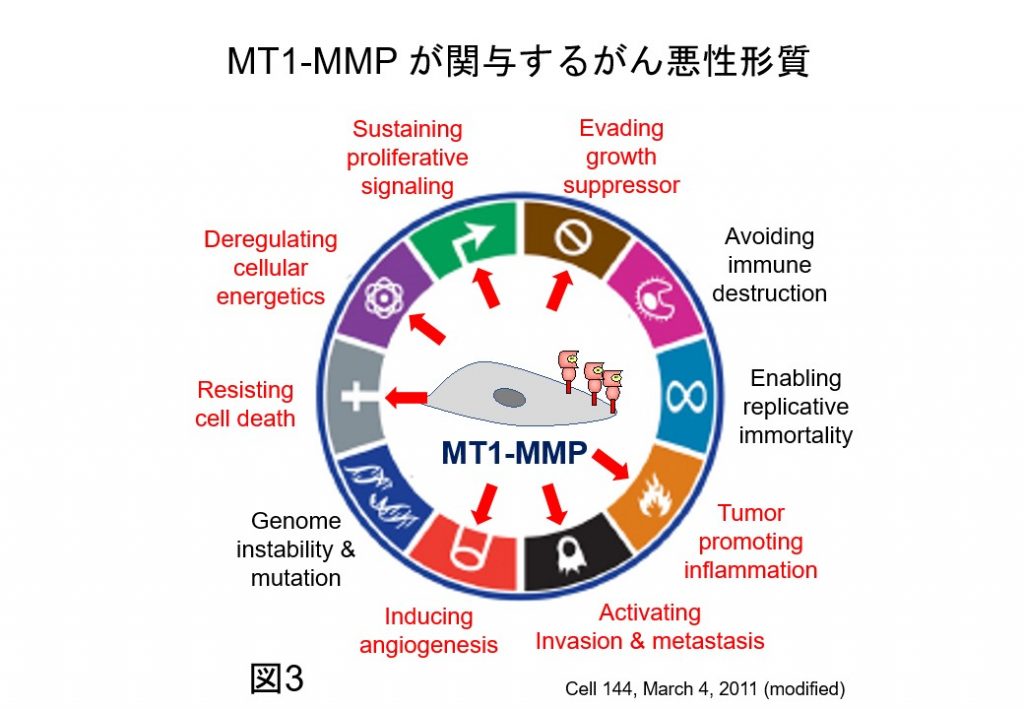
さらに近年、MT1-MMPはがん転移・浸潤だけでなく、がんの多様な悪性形質の獲得に関与することが報告されています(図3)。そのため、MT1-MMPによるがん悪性化進展制御の分子メカニズムを理解することは、新たながん治療法・診断法、創薬を開発することに繋がります。
そこで、私たちは、第3のMT1-MMP基質に着目し、MT1-MMPによるそれら基質の部分切断(プロセシング)が膜蛋白質の新たな機能制御に関与する可能性を系統的に検討しています(図2右)。
これまでに、がん細胞の膜上において、MT1-MMPが、以下の特性を持つことが見出されています(Cancer Sci 2011, Cell Death & Diseases 2017)。
1)がん細胞の悪性化に重要な役割を担う膜型細胞増殖因子やチロシンキナーゼ受容体と相互作用すること(Cancer Sci, 2008)
2)これら膜蛋白質をプロセシンし、その活性を制御することで(Cancer Res 2010, 2015)、がん悪性形質を亢進すること
3)MT1-MMPのプロセシングで生じる基質遊離断片は、がん細胞を生体内で検出するための目印(バイオマーカー)となること
以上より、がん浸潤・転移の動力源として見出されたMT1-MMPは、細胞膜上で様々な膜蛋白質と相互作用することで、がんの多様な悪性形質の獲得に寄与すること、MT1-MMPのプロセシングを受けた膜蛋白質が新たな細胞機能を獲得し、がん治療や診断の新たな標的となることを強く示唆しています。現在、これまでの基礎研究の知見を元にしたトランスレーショナルリサーチを進め、MT1-MMPとその関連分子を標的としたシーズの臨床有用性(Proof of Concept:POC)を得ることで、独創的ながん治療・診断法を社会に向けて発信してゆきます。
健康医療科学分野 教授 越川 直彦
研究目標と内容を簡単に紹介するビデオです




